幹細胞療法による毛髪再生:
臨床エビデンス、再生メカニズム & アジアでのアクセス 2025
推定読了時間: 15~18分
目次
はじめに
脱毛症(alopecia)は世界中で何百万人もの人々に影響を与えており、50歳までに男性の約半数、多くの女性も目に見える薄毛を経験するとされています。自己イメージや自信、生活の質に大きな影響を及ぼし得る症状です。最も一般的なタイプは男性型脱毛症(androgenetic alopecia:AGA)で、遺伝的背景とホルモン要因が関与し、毛包が徐々に縮小して、細く短い毛しか生えなくなっていきます。これに加えて、ストレス、自己免疫反応、特定の医療処置なども、健康な毛髪の成長を妨げる要因となり得ます。
従来の治療法としては、毛包を刺激して成長期を延長する外用薬ミノキシジル(毛包の成長期を延ばし、発毛を促進する外用育毛薬)、DHTホルモン(テストステロンから生成され、男性型脱毛症の原因とされるジヒドロテストステロン)を抑制することで毛包の縮小を防ぐフィナステリド(DHTの生成を抑える内服薬)、さらには自毛植毛手術などがあります。これらは抜け毛の進行を遅らせるうえで一定の効果がありますが、「毛包内の細胞活力の低下」という根本要因までは十分にアプローチできないことも少なくありません。
そこで注目されているのが、幹細胞を用いた再生医療です。毛包微小環境を整え、真皮乳頭細胞の働きを活性化し、自然な組織修復を促進することで、「内側」からより強く健康的な毛髪成長を支えることを目指します。再生医療がアジア各国で進歩する中、マレーシアは科学的根拠に基づいた個別化毛髪再生治療の拠点の一つとして台頭しつつあります。
脱毛症と毛包生物学を理解する
脱毛(alopecia)は、遺伝・ホルモン要因から免疫反応、ストレス、各種医療処置に至るまで、さまざまな要因によって生じ得ます。特に一般的な二つのタイプは、男性型脱毛症(パターン脱毛)と円形脱毛症(スポット脱毛)であり、それぞれ異なる生物学的メカニズムが関与している一方、「毛包の正常な活動が阻害される」という共通の帰結をもたらします。男性型脱毛症(パターン脱毛)
このタイプの脱毛症は主に遺伝的素因とホルモン感受性に関連しています。毛包が徐々に縮小し、細く短い毛しか生えなくなる「毛包ミニチュア化」が特徴です。テストステロンから派生するホルモンであるジヒドロテストステロン(DHT)への感受性が、この過程において重要な役割を果たしていると考えられています。男性では生え際の後退や頭頂部の薄毛として現れやすく、女性では頭頂部全体におよぶびまん性の薄毛として見られます。
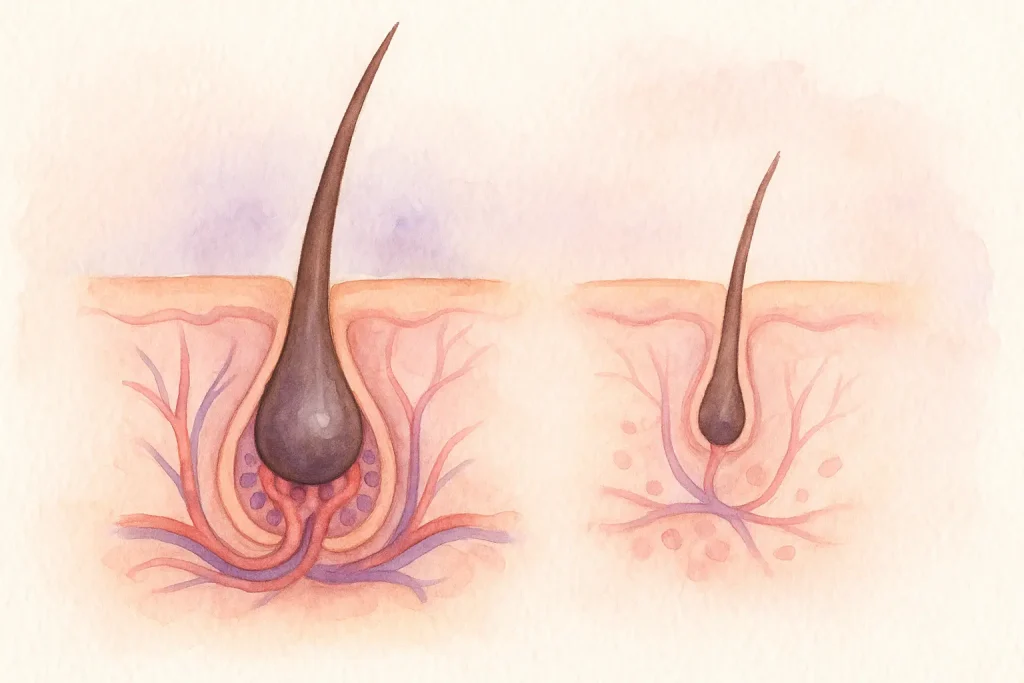
円形脱毛症(スポット脱毛)
円形脱毛症(alopecia areata)は自己免疫疾患の一種であり、免疫システムが誤って毛包を標的として攻撃してしまうことで、頭皮や体の一部に円形の脱毛斑が生じます。場合によっては、頭髪がすべて抜ける全頭脱毛症(alopecia totalis)や、全身の毛が抜ける汎発性脱毛症(alopecia universalis)に進行することもあります。 あらゆる年齢で発症し得て、その経過は予測が難しく、自然に改善する症例もあれば、長期間持続したり再発を繰り返したりする症例もあります。毛周期(ヘアサイクル)
各毛包は、成長、移行、休止、脱落・再生という連続的なサイクルを繰り返しています。主な3つの時期を以下にまとめます。
成長期(アナゲン期)
期間:約2〜7年
頭髪全体の最大90%がこの時期に属し、毛髪が積極的に伸び続ける成長期です。
退行期(カタゲン期)
期間:約2〜3週間
毛包が縮小し、血液供給から切り離され、休止期へ移行する準備をする短い移行期です。
休止期(テロゲン期)
期間:約2〜4か月
毛包が休止し、その後毛髪が自然に脱落して、新たな成長期(アナゲン期)が始まる時期です。
男性型脱毛症では、この成長期が短縮し、休止期が延長することで、徐々に細く弱い毛が増えていきます。円形脱毛症では、免疫活動が毛周期を乱し、毛包が早期に休止・脱落期へ移行してしまいます。
毛包の生物学
細胞レベルで見ると、毛包は継続的な自己再生が可能な「ミニ臓器」ともいえる構造を持っています。毛包基部に位置し毛の成長シグナルを出す真皮乳頭細胞(Dermal Papilla Cells:DPCs、毛の成長を制御する中心的な細胞)や、外毛根鞘細胞などの重要な細胞群が、Wnt/βカテニン、BMP、TGF-βといったシグナル伝達経路を通じて毛包の活動を調節しています。これらは、再生生物学研究において主要な調節因子として繰り返し報告されています。
炎症、酸化ストレス、ホルモンバランスの乱れなどによって、これらの分子経路が障害されると、毛包は再生能力を徐々に失い、休眠状態に移行していきます。毛包微小環境の中で起こる「細胞間コミュニケーションの破綻」は、慢性あるいは進行性の脱毛症における中心的な要因と考えられています。
なぜこの理解が重要か
毛髪成長の背後にある生物学を理解することで、従来の外用薬や内服薬による治療が一時的な改善にとどまりやすい理由が見えてきます。幹細胞ベースの治療は、失われた細胞間シグナルを回復させ、毛包幹細胞を再活性化し、血管新生(アンジオジェネシス:新しい血管の形成)を促進することを目指します。これにより休眠毛包を呼び起こし、より長期的な毛髪再生を支援しようとするアプローチです。
幹細胞療法が毛髪再生にどのように作用するか
幹細胞を用いた毛髪再生療法は、連続的な毛髪成長を支える「毛包微小環境(フォリキュラー・ニッチ)」の修復・若返りに焦点を当てています。休眠毛包を再活性化し、炎症を調節し、血管新生を促すことで、進行性の薄毛の「見た目」を隠すだけでなく、その根底にある生物学的変化にアプローチしようとする点が特徴です。
幹細胞と再生バイオロジクスの種類
毛髪再生のための幹細胞ベース治療には、複数の生物学的に異なる細胞タイプや再生コンポーネントが含まれており、それぞれが毛包の修復や成長に異なる形で寄与します。
間葉系幹細胞
毛髪再生領域で最も広く研究され、臨床利用されている幹細胞で、以下のような組織から得られます。
- 脂肪由来MSCs(AD-MSCs):患者自身の脂肪組織から採取され、毛包回復を刺激する成長因子やサイトカインが豊富です。
- 骨髄由来MSCs(BM-MSCs): 多分化能を持ち、再生および免疫調節機能を有する幹細胞です。
- 臍帯由来MSCs(UC-MSCs): 健康なドナーから得られる同種(アロジェニック)細胞で、免疫適合性が高く、強力な再生シグナルを発することが知られています。
MSCsは主にパラクリン作用(分泌した因子を介した近傍細胞への作用)を通じて働き、炎症調節、血流改善、局所毛包幹細胞の活性化を促す成長因子を放出します。
毛包幹細胞
各毛包の「バルジ領域」(毛包上部にある幹細胞のニッチ)に存在する幹細胞で、毛周期ごとの自然な再生を担う細胞群です。現在の研究では、男性型脱毛症や円形脱毛症において失われた毛包構造を回復させるため、HFSCを再活性化・増幅する手法が検討されています。
多血小板血漿
PRPは患者自身の血液から作られる濃縮製剤で、VEGF、PDGF、IGF-1などの天然の成長因子を高濃度に含みます。これらの成長因子は血流を改善し、毛包活動を刺激し、頭皮内での新たな細胞成長を促します。
PRPはしばしば幹細胞療法と併用され、全体的な結果の底上げや回復の早期化を狙います。PRP自体は厳密な意味での「幹細胞治療」ではありませんが、頭皮の治癒環境を改善し、既存の毛包をより活発にする補完的な役割を果たします。
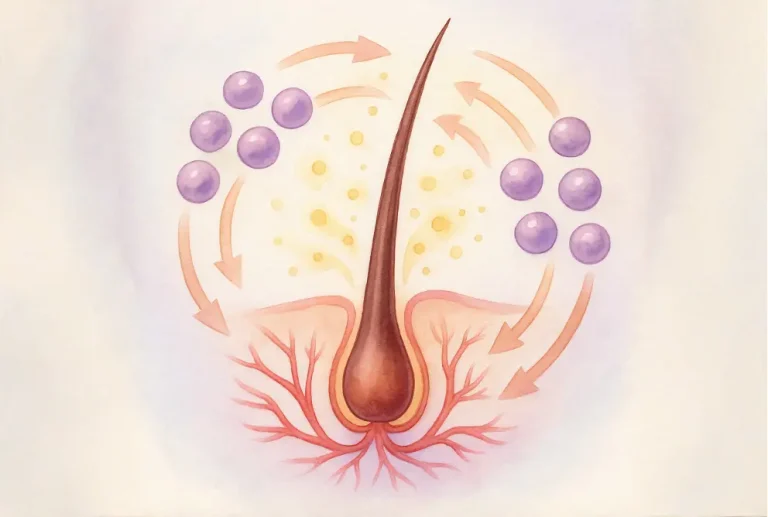
作用メカニズム
幹細胞および再生バイオロジクスは、複数の相補的な生物学的効果を通じて毛髪成長を促進します。
1. 成長因子の分泌
主なシグナル分子には以下が含まれます:
- VEGF(血管内皮成長因子): 血管新生と栄養供給を促進します。
- FGF(線維芽細胞成長因子): 毛包細胞の増殖を刺激し、成長期(アナゲン期)を延長します。
- IGF-1(インスリン様成長因子1): 毛幹の伸長と毛包の生存をサポートします。
- HGF(肝細胞成長因子): 毛包を休止期(テロゲン期)から成長期(アナゲン期)へ移行させることを助けます。
2. 毛包の活性化と増殖
幹細胞は休眠している毛包を再び働かせ、成長シグナルを調節する特化細胞である真皮乳頭細胞を活性化します。これにより、新しい毛幹を形成するマトリックス細胞の増殖が促進されます。
3. 血管新生とコラーゲンリモデリング
再生バイオロジクスは微小循環を改善し、新しい毛細血管の形成を促進するとともに、コラーゲンリモデリングを支援することで、毛包再生に適した酸素と栄養に富む環境を整えます。
4. 抗炎症・免疫調節作用
MSCsはTNF-αやIL-6などの炎症性サイトカインを抑制し、頭皮の炎症を軽減します。円形脱毛症のような自己免疫性疾患では、免疫バランスを再調整し、毛包を免疫媒介性のダメージから保護すると期待されています。
5. 成長期(アナゲン期)の延長
幹細胞由来因子により毛の成長期が長く維持されることで、休止期に入る前により太く長い毛が育つ可能性があります。
6. ミニチュア化の逆転
毛包シグナルと組織の健全性を回復することで、男性型脱毛症の特徴であるミニチュア化した毛包を再び大きくし、その進行を遅らせたり、部分的に逆転させる可能性が示唆されています。
臨床エビデンス:研究が示すもの
安全性プロファイル
- 訓練を受けた医療従事者が無菌環境で施行した場合、幹細胞およびPRPを用いた毛髪再生療法は、臨床研究において一貫して良好な安全性プロファイルを示しています。
- 副作用のほとんどは軽度かつ一時的で、注射部位の軽い発赤や腫脹などにとどまります。
- 最新のDermatologic Therapy(2022)レビューでは、脂肪由来・骨髄由来・臍帯由来MSCsを用いた試験において重篤な有害事象は報告されていませんでした。また、Stem Cells Translational Medicineにおいても、繰り返し投与での高い生体適合性とごく軽微な免疫反応が確認されています。
- 長期データはまだ限られていますが、最大約3年の追跡調査においても安全性が維持されていると報告されています。
有効性に関する知見
男性型脱毛症(AGA)
最近の臨床研究およびメタ解析では、MSCsおよびPRPを用いた治療によって、毛密度・毛径・患者満足度の改善が測定可能なレベルで認められることが示されています。
- PRP(多血小板血漿):2020年の系統的レビューでは、PRPがプラセボまたはミノキシジル対照と比較して毛密度および患者満足度を有意に改善したと報告されていますが、研究間の異質性は依然として高いとされています。[Int J Mol Sci . 2020 – PubMed]
- 脂肪由来幹細胞成分抽出物(ADSC-CE):二重盲検・ビヒクル対照試験では、16週間の外用ADSC-CE適用後に、毛髪本数と太さの両方で統計学的に有意な改善が認められ、優れた安全性と忍容性が確認されました。[J Cutan Aesthet Surg. 2021 – PMC]
- MSCs+PRP併用再生アプローチ:ストローマ血管画分(SVF)で強化したPRPを用いた2025年の研究では、AGA患者での毛密度および頭皮カバー率の増加が報告され、細胞治療と血小板治療を組み合わせた再生アプローチの相乗効果が示唆されています。[Stem Cell Research & Therapy, in press]
現時点のエビデンスから、PRPやADSC-CE、SVF強化PRPなど一部のMSC由来バイオロジクスは、毛密度・毛径・患者満足度の改善に寄与し得ると考えられます。良好な忍容性も確認されています。
しかし、治療プロトコルは研究間で大きく異なるため、大規模で標準化された長期ランダム化比較試験が、結果の有効性と持続性を明確にするうえで今後も必要です。
円形脱毛症(自己免疫性脱毛)
最新の研究では、MSCベース治療が免疫調節や毛包回復を通じて円形脱毛症に効果を示す可能性が指摘されています。例えば、2024年のパイロットスタディでは、局所的なMSC投与後に毛髪の再生および炎症マーカーの減少が観察されました。
一方、PRPに関しては、2022年の系統的レビューで「ステロイドフリーの選択肢となり得る」と評価されていますが、エビデンスの質は限定的であり、反応には個人差が大きいことが指摘されています。[Biomedicines, 2022 – MDPI]
これらの結果は有望ではあるものの、円形脱毛症に対するMSCおよびPRP治療は依然として研究段階であり、日常診療に広く導入するためには大規模ランダム化比較試験(RCT)が必要です。
併用療法および比較研究
- 間葉系幹細胞(MSCs)と多血小板血漿(PRP)を組み合わせた治療は、PRP単独と比較して改善スピードの向上・毛包生存率の増加・移植片の回復促進など、より優れた臨床アウトカムを示すことが報告されています。これらの相乗効果は、幹細胞由来および血小板由来サイトカインによる成長因子シグナルの相補的作用に起因すると考えられています。[Regenerative Therapy, 2022][Cells, 2019]
- 比較試験では、MSCベース治療が外用ミノキシジルと同等あるいはそれ以上の毛密度改善を示し、治療終了後もより長期にわたって効果が持続する可能性が報告されています。[Stem Cell Research & Therapy, 2023]
効果の持続期間
現時点の研究では、幹細胞ベースの毛髪再生療法について、短〜中期的な安全性と有効性は支持されていますが、長期的な持続性はなお検証段階です。以下に、公開されている臨床研究から一貫して報告されている主なポイントをまとめます。
サンプルサイズの小ささ
多くの臨床試験は10〜50名程度にとどまり、統計的な力と一般化可能性が限定的です。
追跡期間の制限
多くの研究で追跡期間は6〜24か月にとどまり、3年以上の長期追跡データはごく少数です。
プロトコルの多様性
細胞ソース、細胞数、投与濃度、セッション頻度などが研究・施設ごとに大きく異なり、比較が難しい状況です。
反応のばらつき
約60〜70%の患者で目に見える改善が報告される一方、効果が限定的または最小限にとどまる例もあります。
標準化の必要性
最適な投与量、治療間隔、長期維持効果を明確にするため、多施設共同の大規模ランダム化比較試験が求められています。
近年のコンセンサス
系統的レビューでは、一貫した短期的メリットは認められるものの、2〜3年以上の長期アウトカムについてはさらなるエビデンスが必要とされています。
総じて、幹細胞ベースの毛髪再生療法は短〜中期的な良好な結果を示していますが、真の長期的持続性については今後の研究が継続されています。
既存治療との比較
以下は、従来療法と再生医療アプローチの比較であり、作用機序、限界、効果の持続期間の違いを整理しています。
主な作用機序: 頭皮血流を改善し毛包を刺激
主な限界: 継続使用が必要
効果の持続期間: 一時的
主な作用機序: DHTホルモンの産生を抑制
主な限界: ホルモン関連の副作用、主に男性のみ
効果の持続期間: 継続的
主な作用機序: 血小板由来成長因子による刺激
主な限界: 効果持続が短く、反応に個人差
効果の持続期間: 約6〜12か月
主な作用機序: 毛包を移植する外科的治療
主な限界: ドナー部位の制限、ダウンタイムが必要
効果の持続期間: 移植毛は基本的に恒久的
主な作用機序: 毛包微小環境の再生、免疫調節
主な限界: 研究段階であり、複数回セッションが必要なことが多い
効果の持続期間: 約12〜18か月の可能性
アジアにおけるアクセスと規制状況
規制の概要
- 日本:再生医療安全性確保法のもと、多くの民間クリニックで実施されるMSC手技は自家(オートロガス)細胞が中心です。一方、同種(アロジェニック)MSCの使用は、特定の承認製品または臨床試験に限定されます。
- 韓国:病院主体のMSC療法は主に自家細胞が用いられ、同種MSC製品の使用は再生医療関連法規により厳格に管理されています。
- マレーシア:保健省(MOH)の幹細胞/CGTPガイドラインのもと、ライセンスを取得した施設では、ワートンジェリー由来WJ-MSCsを含む培養同種MSCsを、政府主導・ガイドライン準拠の枠組みの中で臨床利用することが可能です。
- シンガポール・タイ:MSC療法は細胞/組織/遺伝子治療製品として認定施設で管理されており、培養同種MSCへのアクセスは、登録済み製品や正式な臨床試験に比較的限定され、医療ツーリズム向けに広く提供されているわけではありません。
この中で、マレーシアはワートンジェリー由来WJ-MSCsなどの培養同種MSCsが、明確な国家ガイドラインのもとで患者に提供されている国の一つです。
アクセスと臨床実務
治療は通常、再生医療専門クリニックや皮膚科クリニックなど、専門性の高い施設で行われます。MSC製剤はマイクロインジェクション(頭皮への局所注射)や点滴投与などの形で外来ベースで投与されることが多く、治療前には安全性と適応を確認するため、頭皮画像検査や血液検査が実施されます。
保険適用と費用
多くのアジアの保険会社はMSC療法を「研究段階の治療」と位置づけています。そのため通常は自由診療となり費用は自己負担ですが、一部のプレミアム保険や国際医療保険プランでは、部分的な補償が行われる場合もあります。
費用は細胞ソースやセッション数によって幅がありますが、一般的に日本や韓国と比較すると、マレーシアやタイの方が費用面でアクセスしやすい傾向があります。
利点と限界
幹細胞ベースの毛髪再生療法には再生医療としての利点がある一方、臨床的・実務的な限界も存在します。以下は、エビデンスに基づいてバランスよく整理した概要で、治療判断の一助となることを目的としています。
期待される利点
- 非外科的かつ低侵襲な処置であること
- 自然な毛包再生と頭皮若返りを促す可能性
- 時間の経過とともに毛密度、毛質、全体的な髪の質感が改善し得ること
- ダウンタイムが少なく、PRPや低出力レーザー療法など他の毛髪治療と併用しやすいこと
- フィナステリドと異なり、全身ホルモンレベルを直接変化させない点
主な限界
- 臨床エビデンスは依然として発展途上であり、効果は個々の反応や疾患ステージによって異なる
- 生きた毛包がほとんど残っていない「完全なつるつる状態」には効果が乏しい
- 最適な結果を維持するには、定期的なメンテナンスセッションが必要となる場合が多い
- 費用・アクセス性・規制状況はアジア各国で異なり、すべての国で同様に利用できるわけではない
幹細胞ヘアリストレーションの未来
ヘアサイエンスおよび臨床皮膚科の分野では、次世代の再生アプローチが急速に発展しています。
- エクソソームベース療法:成長因子、サイトカイン、RNA分子に富む無細胞小胞(エクソソーム)を利用し、細胞そのものを移植することなく毛包再生シグナルを届ける細胞フリー治療。
- 3D毛包オルガノイド研究:幹細胞から実験室内で機能的な「ミニ毛包(オルガノイド)」を再構築し、新規毛包を作り出すデノボ毛包形成を目指す研究。
- 遺伝子編集MSC:Wnt/βカテニン経路の活性化など、毛包の成長と寿命を高めることを目的として設計されたMSCの検討。
- シナジーを狙った併用プロトコル:MSCとPRP、マイクロニードリング、低出力レーザー療法などを組み合わせ、頭皮の再生と毛密度の改善を最大化しようとするアプローチ。
これらの革新的な取り組みにより、幹細胞を用いた毛髪治療は「実験的介入」から「構造化されたエビデンスベースの再生皮膚科」へと進化しつつあります。アジアにおいても、その標準化と適切な普及が期待されています。
よくある質問(FAQ)
幹細胞を用いた毛髪再生に関するよくある質問について、適応、 安全性、そしてアジア各国でのプロトコルの違いなどを、エビデンスに基づいて分かりやすくまとめています。
マレーシアでは、再生医療は2021年の「National Cell and Gene Therapy Guidelines」に基づいて規制されています。ライセンスを受けたクリニックは、臨床プロトコルの中で皮膚科領域のMSCベース治療を提供することが可能ですが、これらの治療は依然として「研究段階(investigational)」と位置づけられており、標準治療として完全に承認されているわけではありません。
多くの研究では、目に見える改善が概ね12〜18か月持続すると報告されています。結果を維持するため、9〜12か月ごとのメンテナンスセッションが推奨されることもあります。
理想的な候補者は、生きた毛包が残っている部分的な薄毛の方で、一般的には初期〜中等度の男性型脱毛症、あるいは自己免疫関連のパッチ状脱毛などが含まれます。活動性毛包がほとんど残っていない完全な脱毛状態では、反応性が低い傾向があります。
はい、併用は可能です。MSCとPRPを組み合わせることで、相補的な成長因子シグナルと頭皮治癒促進効果により、より速く、かつ持続的な毛髪再生が得られる可能性があります。
多くの患者では、1〜3日程度の軽い赤みや腫れ、圧痛などにとどまり、通常は治療直後から日常生活に復帰できます。
報告されている副作用の多くは軽度で、一時的な頭皮の痛みや熱感などです。適切に認定された施設で無菌操作のもと実施される限り、重篤な合併症はまれとされています。
臨床プロトコルは国によって多少異なります。日本と韓国は厳格な再生医療法制に基づいており、マレーシアとタイではライセンス制の細胞治療プログラムを通じてアクセスが提供されています。治療前には、受診予定のクリニックが適切に認定されているか必ず確認してください。
はい、可能です。MSCおよびPRP療法は、特に更年期以降やストレス関連の女性型薄毛において有効性を示した研究報告があります。
現時点のエビデンスでは、18〜24か月程度の持続的な効果が報告されていますが、「生涯にわたる永久的効果」と言えるかどうかについては、まだ臨床研究の途上です。
結論
幹細胞療法は、毛包構造そのものの再生を目指す「生物学的に修復的なアプローチ」であり、表面的な刺激にとどまらない、毛髪喪失の管理における新たな選択肢として位置づけられます。初期の臨床報告では、毛密度、頭皮状態、患者報告ベースの満足度などにおいて測定可能な改善が認められ、全体として良好な安全性プロファイルに支えられています。
一方で、幹細胞ベースの毛髪再生は依然として新興領域であり、長期的な有効性や最適なプロトコルに関しては、今後の研究の蓄積が求められています。患者は、再生医療に精通した専門医に相談し、クリニックの認定状況や治療プロトコルを確認したうえで、結果に対して現実的な期待値を持つことが推奨されます。
科学的理解と臨床標準化が進むにつれ、MSCを中心とした再生療法は、アジア全域における総合的な毛髪治療戦略の重要な一部となっていく可能性があります。ご自身の症状に再生医療アプローチが適しているか知りたい方は、認定された医療機関の専門家にご相談いただくか、当院までお気軽にお問い合わせください。
科学的参考文献
- Dermatologic Therapy (2022). Safety review of adipose-, bone marrow–, and umbilical cord–derived MSCs in dermatology. PubMed 35948034
- Stem Cells Translational Medicine. Biocompatibility and immune tolerance of repeated MSC applications. PubMed 30723013
- International Journal of Molecular Sciences (2020). Systematic review of PRP efficacy for androgenetic alopecia. PubMed 32295047
- Journal of Cutaneous and Aesthetic Surgery (2021). ADSC-CE double-blind clinical trial for hair density improvement. PMC 8611710
- Stem Cell Research & Therapy (2025, in press). Stromal vascular fraction (SVF)–enhanced PRP for androgenetic alopecia. 10.1186/s13287-025-04560-7
- International Journal of Molecular Sciences (2024). MSC pilot study for alopecia areata and immunomodulation. PubMed 39273184
- Biomedicines (2022). Systematic review of PRP as a steroid-free option for alopecia areata. Biomedicines 2022;10(8):1829
- Regenerative Therapy (2022). MSC + PRP combination therapy improving graft survival and clinical recovery. S2352-3204(22)00102-X
- Cells (2019). Clinical outcomes of MSC and platelet-derived product synergy in hair restoration. PubMed 31100937
- Stem Cell Research & Therapy (2023). Systematic review on MSC-based therapies for hair loss and long-term outcomes. 10.1186/s13287-023-03440-2
ℹ 免責事項
本記事は情報提供および教育目的のみを意図しており、医療上の助言、診断、または治療の推奨を構成するものではありません。脱毛に対する幹細胞療法は新興分野であり、最適なプロトコル、長期的な安全性、臨床的有効性に関しては現在も研究が継続中です。治療の提供状況、法的な位置づけ、臨床標準は国や医療機関によって異なります。個々の治療結果は患者固有の要因に左右され、保証することはできません。
治療に関する意思決定を行う前に、皮膚科専門医や再生医療専門医など、必ず有資格の医療専門職にご相談ください。ここで示される情報は、査読付き科学文献および臨床経験に基づく2025年11月時点の知見を反映しており、新たな研究の進展に伴い変更される可能性があります。
最終更新日:2025年11月