歯の再生幹細胞療法:2025年総合ガイド
推定読了時間: 10~12分
目次
はじめに
歯の喪失や歯の組織損傷は、これまで長い間、疾患、外傷、あるいは加齢によって避けられないものと考えられてきました。詰め物、根管治療、インプラントなどの従来の歯科治療は、形態や機能を回復させるうえで有効ですが、生きた組織そのものを再生することはできません。
近年、歯の再生幹細胞療法の進歩により、新たな可能性が開かれました。それは、幹細胞を用いて歯そのものの生体構造を修復・再生するというアプローチです。失われたものを単に置き換えるのではなく、歯の内部にある自然な活力、血流、防御機構を蘇らせようとする試みです。幹細胞を応用した歯科治療は、この変革の最前線に立っています。根管治療後の歯髄の再生から、歯周病によって損傷した歯周組織の再構築まで、これらの治療法は歯科医療における「治癒」の概念を再定義しつつあります。
本ガイドでは、世界でも最も先進的な再生歯科研究が進められているアジア地域における、最新の臨床エビデンス、進行中の研究、そして実際の臨床応用について包括的に紹介します。

歯科幹細胞療法とは?
歯科幹細胞療法は、主に歯髄幹細胞(DPSC:Dental Pulp Stem Cells)といった特殊な細胞を用いて、損傷した歯の組織を修復・再生する治療法です。これらの幹細胞は、次の部位から採取することができます:
- 歯髄(歯の内部にある軟組織)
- 歯根膜(歯と骨をつなぐ組織)
- 根尖乳頭(発育中の歯根先端にある組織)
- 歯肉組織(歯ぐきの組織)
- 脱落した乳歯(SHED細胞として知られる)
胚性幹細胞とは異なり、歯科幹細胞は倫理的な懸念が少なく、抜歯した親知らずや自然に脱落した乳歯から比較的容易に採取できます。
作用の仕組み
損傷した歯の組織に導入された幹細胞は、必ずしも直接新しい歯や歯髄に変化するわけではありません。主に次のような仕組みを通じて治癒と再生を促します:
- パラクリンシグナリング:成長因子を放出し、修復と再生を促進する
- 細胞分化:象牙芽細胞(象牙質を形成する細胞)やその他の歯科特化細胞へ分化する
- 抗炎症作用:組織の炎症を抑え、治癒に適した環境を整える
- 血管新生:新しい血管の形成を促し、血液供給を回復させる
現在の臨床応用
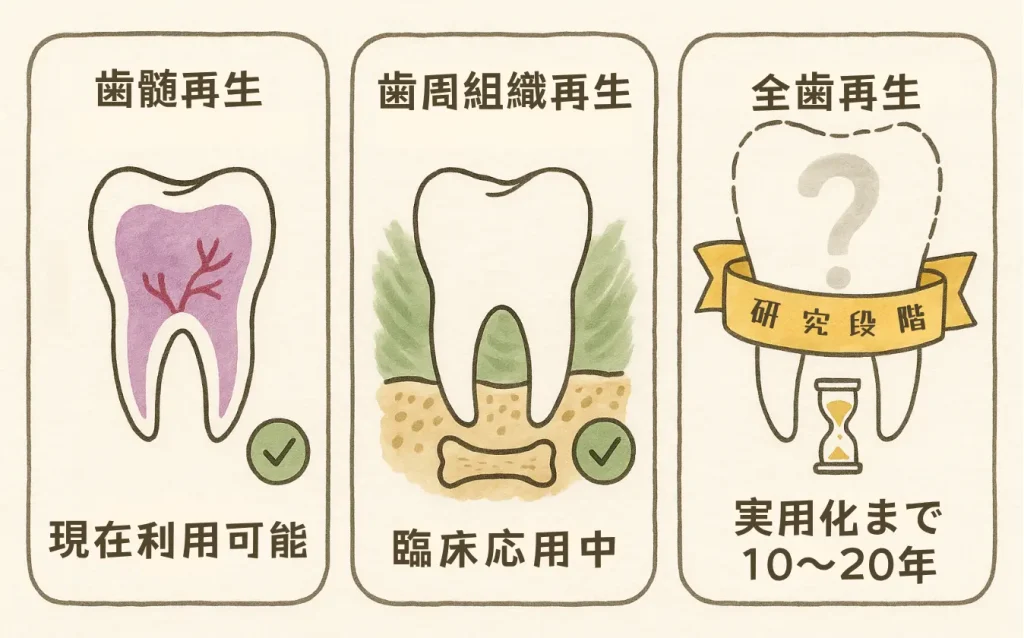
1. 歯髄再生(歯内治療の再生)
課題:従来の根管治療では、感染した歯髄を除去するため、歯は感覚・血流・自然な防御機構を失い、「死んだ状態」となります。
解決策:幹細胞療法は、機能的な歯髄組織の再生を目指し、治療後も歯が生きた状態で維持される可能性を開きます。
臨床エビデンス:
- 日本のパイロット臨床研究では、自家歯髄幹細胞(DPSC)を抜髄歯に移植した結果、4週間以内に電気歯髄検査(EPT)で陽性反応が得られ、MRIで歯髄様組織の形成が確認されました。[Stem Cell Research & Therapy, PubMed]
- 脱落乳歯由来の自家幹細胞(SHED)を損傷した未成熟永久歯に移植したところ、血管および神経を含む歯髄様組織が再生しました。[Science Translational Medicine, DOI: 10.1126/scitranslmed.aaf3227]
- 40名(治療群30名+対照群10名)を対象とした前向き無作為化比較試験では、SHED治療により血管再生、電気刺激への反応、歯根長の増加が12か月時点で確認され、副作用は報告されませんでした。一部の患者は最大24か月追跡され、安全性が確認されています。[World Journal of Stem Cells, DOI: 10.4252/wjsc.v15.i3.31]
現状: 日本や中国を中心に複数の臨床試験が進行中ですが、歯髄再生は依然として実験段階にあり、GMP準拠の専門施設が必要です。現時点では標準治療には至っていません。
2. 歯周組織再生
課題:歯周病は歯を支える歯肉、靭帯、骨などの支持組織を破壊し、歯の喪失を引き起こします。従来の治療は進行を抑えることはできますが、失われた歯周組織を再生することは難しいとされています。
解決策:幹細胞療法は、歯周靭帯、歯槽骨、歯肉組織を再構築できる再生細胞を注入または移植し、支持組織の回復を目指します。
臨床エビデンス:
- 中国の慢性歯周炎患者132名を対象とした多施設共同無作為化臨床試験では、歯髄幹細胞(DPSC)の注射により、骨欠損の改善幅は幹細胞注入群で平均0.30mmと、比較対照の生理食塩水注射群(0.04mm)より明らかに大きい結果が得られました。特にステージIIIの患者で最も顕著な効果が認められました。[Signal Transduction and Targeted Therapy, PubMed]
- 自家DPSCマイクログラフトとコラーゲンスポンジを併用した無作為化対照試験では、12か月後にコラーゲン単独群と比較して、プロービング深度の減少、臨床的付着の増加、骨充填が有意に改善しました。[Journal of Clinical Periodontology, PubMed]
- 脱臼歯患者15名を対象としたパイロット研究では、生体工学的微小環境内に乳歯歯髄幹細胞(hDPSC)凝集体を移植した結果、歯周組織の機能的再生と歯根の継続的成長が観察されました。[Biomaterials, PubMed]
現状: 歯周組織再生は歯髄再生よりも臨床応用が進んでおり、複数の研究で構造的・臨床的改善が示されています。ただし、手技や条件は標準化されておらず、多くの応用はアジア地域の研究機関や専門再生医療施設に限られています。
3. 歯全体の再生(実験段階)
究極の目標:失われた歯を新しい生体歯で置き換えること。
現実:実験動物では歯様構造の生成に成功していますが、人間での完全な歯再生はまだ実験段階にあり、臨床利用は実現していません。
研究の進展:
- マウスで歯芽形成が確認されています。
- 幹細胞とスキャフォールドを組み合わせた生体工学的歯構造が有望視されています。
- 主な技術的課題:
- 適切な形状の歯の形成
- 正確な位置付けと組織統合の確保
- 機能的なエナメル質形成の達成
- 神経・血管接続の確立
現状: 専門家の多くは、臨床応用まで少なくとも10〜20年かかると予測しています。現在の研究の焦点は、歯全体の再生ではなく、歯髄や歯周組織などの組織特異的な再生に置かれています。
臨床エビデンス:研究で示されていること
安全性プロファイル
動員型歯髄幹細胞(MDPSC)移植に関する臨床評価では、治療を受けた患者で有害事象や毒性は報告されていません。歯科領域の複数研究から、次の点が示されています。
- 合併症率が低い:副作用は最小限で、多くは軽度で一時的な不快感にとどまる。
- 重篤な有害事象なし:腫瘍形成、免疫拒絶、重篤な反応の報告なし。
- 良好な忍容性:多くの患者が重大な合併症なく処置を受けている。
例えば、抜髄後の歯に自家MDPSCを移植したヒトのパイロット研究では、重篤な副作用は報告されず、歯髄様組織の形成が確認されています。[Stem Cell Research & Therapy, PubMed]
有効性の知見
2024年の系統的レビューでは、歯の再生幹細胞療法におけるヒト臨床試験における歯由来間葉系幹細胞の治療的利用を検討し、歯髄再生、歯周修復、さらには全身性疾患への応用に関心が広がっていること、短期の安全性・有効性が概ね良好である一方、長期エビデンスや標準化された臨床プロトコルは依然として限られることが指摘されています。[Journal of Dental Research, DOI: 10.1177/00220345241261900]
主な観察結果:
- 歯髄再生: 新生血管形成を伴う歯髄様組織の再構築が報告。[Tissue Engineering & Regenerative Medicine, PubMed / DOI: 10.1007/s13770-021-00389-2]
- 歯周の改善: 慢性歯周炎に対するDPSC注射を用いた多施設RCTで、付着レベルや骨欠損深さの有意な改善が観察。[Signal Transduction and Targeted Therapy, PubMed / DOI: 10.1038/s41392-025-02320-w]
- 歯の感覚: 自家歯髄幹細胞を用いた小規模パイロット研究で、非生活歯における感覚(電気刺激への反応)の回復が報告。[Stem Cell Research & Therapy, PubMed]
- 歯根発育: SHED移植後、未成熟永久歯で歯根の継続的成長が観察。[Science Translational Medicine, DOI: 10.1126/scitranslmed.aaf3227]
重要な限界
これらの励みになる知見にもかかわらず、研究者は、明確な長期的費用対効果のエビデンスと、従来の治療を超えた歯の保持改善の証明は依然として限られていることを強調しています。
- ほとんどの臨床研究は小さなサンプルサイズ(5〜50人の患者)と短期フォローアップを含みます。[International Journal of Molecular Sciences, DOI: 10.3390/ijms22094357]
- 長期データ(5〜10年)はまだ不足しています。
- 研究間でプロトコルが異なり、比較が困難です。
- 結果は患者の年齢、疾患の重症度、全身の健康状態によって異なります。
治療プロセス
治療前評価
治療を受ける前に、患者は通常次のような検査・評価を行います。
- 包括的な歯科検査
- 放射線画像検査(X線、CBCT、必要に応じてMRI)
- 歯の生活状態と疾患の重症度の評価
- 病歴の確認
- 治療に対する期待や代替案についての説明
細胞採取
自家治療(患者自身の細胞を使用する場合)
- 親知らず、または適切な歯を抜歯
- 無菌環境下で歯髄組織を採取
- GMP認証施設で細胞を分離・培養
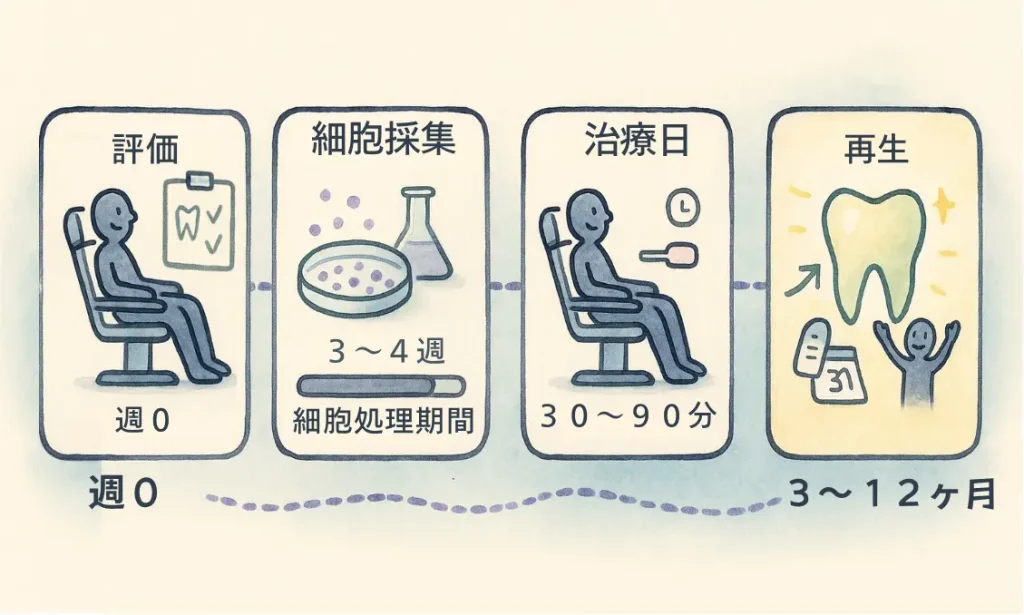
- 細胞の培養には通常3〜4週間を要します
同種治療(ドナー細胞を使用する場合)
- 組織バンクで事前に処理された幹細胞を使用
- 寄付された臍帯、乳歯、または成人歯組織に由来
- 品質検査済みで、即時使用が可能です
細胞投与
病状や治療目的に応じて、次の方法で細胞を導入します。
- 歯髄再生: 洗浄済みの根管内に、幹細胞と足場(スキャフォールド)材料を注入
- 歯周組織再生: 患部歯肉への注入、または膜を併用した外科的移植
- 通常、処置は局所麻酔下で実施されます
- 治療時間の目安は約30~90分です
治療後のケア
- 定期的なフォローアップ(経過観察の診察)
- 画像検査による組織再生の確認
- 合併症の有無のモニタリング
- 標準的な口腔衛生の維持
- 治療効果は通常6~12か月をかけて評価されます
アジア地域における歯科幹細胞治療の現状
歯科幹細胞治療の提供状況は、アジア各国で研究段階、規制体制、臨床導入の進展度が異なります。これは、各国の再生医療に関する研究環境と政策の成熟度を反映しています。
臨床治療を実施している国
- 日本: 歯髄再生研究および初期臨床応用の分野で世界をリードしています。
- 中国: 歯科幹細胞を用いた歯周組織再生を提供する医療施設が複数存在します。
- 韓国: 高度な研究インフラを有し、一部施設で臨床応用が進行しています。
- タイ: 再生医療を取り入れた歯科ツーリズム拠点として台頭しています。
- シンガポール: 主に研究を中心とし、限定的ながら厳格に管理されたパイロット治療を実施しています。
- マレーシア: 再生歯科への関心が高まっており、現時点では研究および実証プログラムに限定されています。
規制に関する考慮事項
治療基準や承認プロセスは国によって異なります。
患者は治療を検討する際、次の点を確認することが推奨されます。
- 各国の保健当局による監督: 例)マレーシア保健省、日本のPMDA、米国FDAなど
- GMP認証を受けた細胞加工・管理施設を利用していること
- 再生医療の専門教育を受けた認定歯科医師が実施していること
- プロトコルの透明性、患者のインフォームドコンセント、適切な経過フォローが確保されていること
利点・リスク・制限
潜在的な利点
生物学的な修復
- 「死んだ歯」を作るのではなく、歯の生活力を維持できる可能性があります。
- 自然治癒や歯の発育の継続が期待されます。
- 知覚や防御機構の回復が見込まれます。
低侵襲性
- 従来の外科的処置よりも侵襲が少ない場合が多く、
- 一部の従来治療と比べて回復が早い傾向があります。
- 抜歯を回避できる可能性があります。
長期的な展望
- 将来的な再治療や介入の必要性を減らす可能性があります。
- 既存の組織との生物学的統合が期待されます。
- 時間の経過とともに機能の改善が持続する可能性があります。
リスクと副作用
一般的(軽度)
- 一時的な違和感や知覚過敏
- 治療部位の軽度な腫れ
- 一時的な炎症
まれだが起こりうるリスク
- 無菌操作が守られなかった場合の感染
- 治療効果が得られないケース(研究によっては患者の20〜40%で報告)
- 予測困難な治療結果
未知の要因
- 長期的な安全性(10年以上)はまだ確立されていません。
- 予期せぬ組織反応が起こる可能性があります。
重要な限界
臨床的限界
- 確実な効果を保証する治療ではありません。
- すべての歯科疾患に適用できるわけではありません。
- 再治療や複数回の施術が必要となる場合があります。
- 成功率は残存組織の健康状態に大きく依存します。
実際的な限界
- 大学病院や再生医療専門センター以外では提供が限られています。
- 保険適用外の場合、費用が高額になることがあります。
- 専門的な施設と高度な技術を持つ医療従事者が必要です。
- 自家細胞治療では、細胞培養に数週間を要します。
科学的限界
- 最適なプロトコルは現在も検証・改良が進められています。
- 使用する細胞の種類・量・投与方法は研究段階にあります。
- 患者ごとの反応には個人差があり、予測は困難です。
治療の適応となる可能性
歯科幹細胞治療は、次のような患者に適している場合があります。
適している可能性が高い方
- 歯髄が壊死しているものの、それ以外の歯は健康な方
- 中等度の歯周病を有する方
- 自然の歯をできるだけ保存したいと考えている方
- 未成熟な永久歯に治療が必要な方
- 細胞採取に適した歯(例:親知らずなど)を有する方
- 治療がまだ実験的段階であることを理解し、定期的な経過観察に協力できる方
治療が推奨されない方
- 歯の構造的損傷が著しく、修復が不可能な場合
- 重度の歯周病で広範な骨吸収が進行している場合
- 活動性の口腔感染がある場合(まず感染を制御する必要があります)
- 治癒能力に影響を与える全身性疾患を有する場合
- 適切な口腔衛生管理を維持できない方
- 確実な結果を期待している方(効果には個人差があります)
- 即効性のある結果を求める方(再生には数か月~1年程度を要します)
今後の展望:歯科再生医療の未来
新たに登場するテクノロジー
組織工学の進歩
- 天然の歯構造を再現する3Dバイオプリント足場材
- 必要に応じて成長因子を放出するスマートバイオマテリアル
- 再生能力を高めた遺伝子改良型幹細胞
細胞治療の進化
- 幹細胞そのものを使用せず、細胞由来のエクソソームを活用するセルフリー治療
- 成長因子やバイオマテリアルを併用した複合再生療法
- 誰でも使用できる標準化された「オフ・ザ・シェルフ」型幹細胞製剤の開発
全歯再生への挑戦
- バイオエンジニアリングによる人工的な歯胚(しはい)の形成研究
- 歯胚移植技術の開発
- 長期的には、インプラントに代わる生物学的な歯の再生を目指す
現実的な見通し
研究は急速に進展していますが、患者は次の点を理解しておくことが重要です。
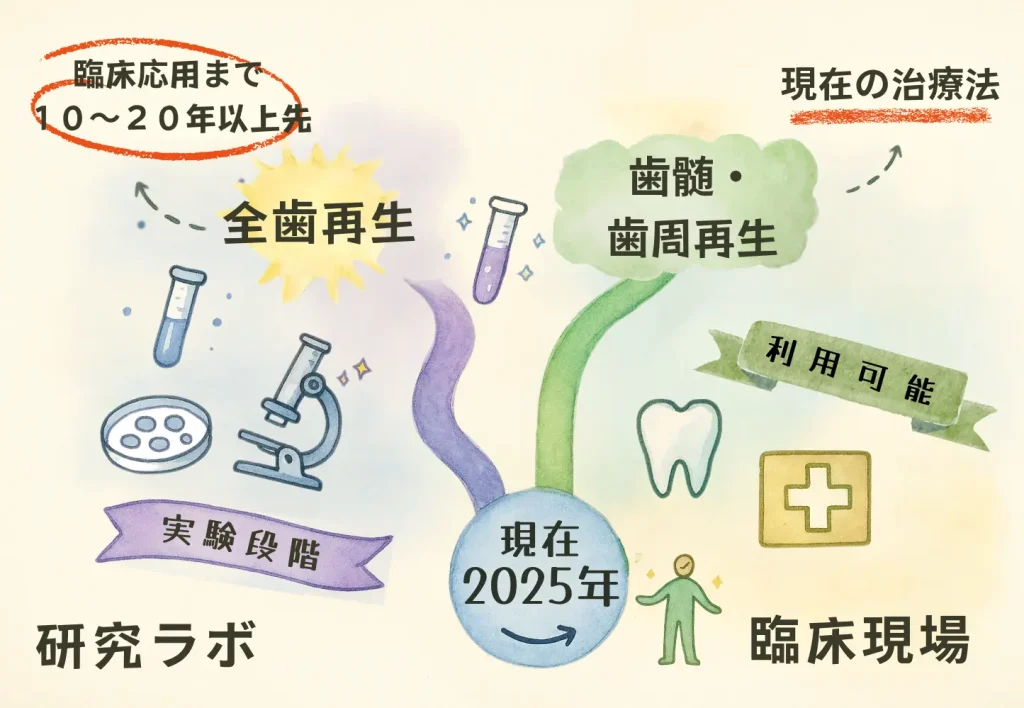
- 全歯の再生は依然として実験段階にあり、臨床応用までには数十年を要する見込みです。
- 現在の応用範囲は、歯髄や歯周組織など一部の組織再生に限定されています。
- 技術は進化を続けていますが、規制当局の承認には時間がかかります。
- 現在の実験的治療が将来的に標準治療となる可能性はありますが、その歩みは段階的です。
よくある質問(FAQ)
Q1:幹細胞で新しい歯を生やすことはできますか?
まだできません。全歯の再生(ホールトゥース・リジェネレーション)は現在も研究段階にあり、臨床応用までには数年から数十年を要すると考えられています。
Q2:歯科幹細胞治療は安全ですか?
臨床研究では、重篤な副作用がほとんど見られない良好な安全性が確認されています。ただし、長期的なデータ(5〜10年以上)はまだ限られています。治療は、認可を受けた医療機関で適切な監督のもとに受けることが重要です。
Q3:効果が現れるまでどのくらいかかりますか?
再生はゆるやかに進みます。数週間以内に初期変化が見られることもありますが、本格的な組織再生には3〜6か月、さらに12〜24か月かけて改善が続く場合もあります。
Q4:保険は適用されますか?
現時点では、多くの保険会社が歯科幹細胞治療を「実験的治療」として扱っており、**保険適用外(自費診療)**となるのが一般的です。
Q5:どこで歯科幹細胞治療を受けられますか?
国や治療内容によって異なります。日本・中国・韓国では比較的臨床経験が豊富です。受診の際は、施設の認可状況や規制遵守の有無を必ず確認してください。
Q6:子どもの乳歯を将来のために保存できますか?
はい。いくつかの民間企業が、乳歯から幹細胞を採取・保存する**バンキングサービス(歯髄幹細胞保管)**を提供しています。保存には年間の保管料がかかります。
Q7:歯科インプラントとどう違うのですか?
インプラントは、失った歯を人工的に補う確立された治療法です。一方で幹細胞治療は、歯や周囲の組織をできるだけ保存・再生することを目的としており、両者は代替関係ではなく、異なる役割を持つ治療法です。
Q8:成功率はどのくらいですか?
治療内容や患者さんの状態によって異なりますが、研究では歯髄再生で60~80%程度の良好な結果が報告されています。歯周組織の再生では、さらに高い成功率が示されています。ただし、個人差が大きいことも指摘されています。
結論
歯の再生幹細胞療法は、「機械的な修復」ではなく「生物学的な再生」を実現する、歯科医療における新たな最前線です。アジア各国および世界で行われている臨床試験の結果からは、特に歯髄再生や歯周組織再生といった分野で有望な成果が報告されています。しかし、現時点ではまだ一般的な治療法とは言えず、全歯の再生(ホールトゥース・リジェネレーション)は将来的な目標にとどまっています。過度な期待を持たず、現実的な理解を持つことが大切です。
歯科幹細胞治療を検討する際は、以下の点にご注意ください。
- 再生歯科医療に関する専門知識と経験を有する歯科医師に相談する
- 医療機関の認可や、国の規制・ガイドラインに準拠しているか確認する
- 現在の治療がまだ臨床研究段階にあることを理解する
- 実績のある従来治療(根管治療・歯周再生治療など)を第一選択肢として検討する
- 幹細胞治療を補助的または将来的な選択肢として位置づける
研究の進展と技術の発展により、幹細胞を用いた再生治療は今後さらに洗練され、より安全で身近な医療技術となることが期待されます。まだ「新しい歯を育てる」段階には至っていませんが、歯の損傷や疾患に対する治療の在り方が大きく変わりつつあることは確かです。再生歯科や幹細胞治療に関心をお持ちの方は、信頼できる歯科専門医にご相談のうえ、最新の研究動向や治療選択肢について情報を得てください。
ℹ 免責事項
本記事は、情報提供および教育を目的として作成されたものであり、医療または歯科診療に関する助言を行うものではありません。幹細胞を用いた歯科治療は、依然として研究段階にある実験的治療であり、その安全性・有効性・規制当局による承認については、現在も研究および検証が続けられています。治療の提供状況や法的な位置づけ、標準的な手順は国や医療機関によって異なります。また、治療の結果は患者一人ひとりの状態により異なり、効果を保証するものではありません。いかなる治療を検討する場合も、必ず資格を有する歯科医師または医師にご相談ください。
最終更新日:2025年10月